质量管理
-
2021.04.20
【独家】医疗器械领域人工智能技术的发展
人工智能在医疗机械中的应用正在不断增加。尽管还没有具体的指令或监管框架,但AI决策仍然需要加以理解和验证,以确保患者的安全……

阅读更多 -
2021.03.23
包装应成为设计控制过程的一部分
Oliver Healthcare Packaging公司产品营销总监Jenn Goff认为,在医疗器械产品设计过程中应尽早考虑包装设计因素,这一点是非常重要的。她在采访中分享了有关包装设计控制要求的技巧……

阅读更多 -
2021.03.19
有源医疗器械的电气安全
医疗器械在诊断、治疗、监护方面发挥着重要作用,其中绝大部分以电源为能源动力,被称为有源医疗器械。而有源医疗器械的准确定义……
阅读更多 -
2021.03.04
可降解镁金属骨科植入物注册技术审查要点探讨
同时镁金属可以和体液发生化学作用,通过腐蚀逐步降解为离子状态,避免了部分植入产品二次取出的风险。因此近些年可降解金属研究是一个热点,生物可降解金属材料文献数量迅速增长……
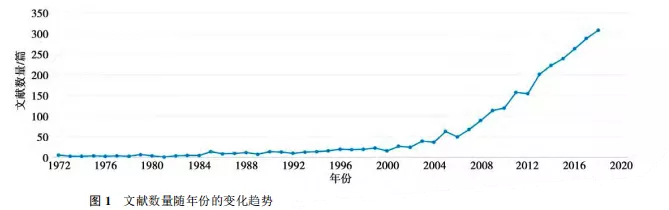
阅读更多 -
等同!等同!到底怎么样才算等同?
最早,在医疗器械指令(MDD93/42/EEC)中提出了等同的概念,随后2016年6月,欧盟发布了关于医疗器械临床评估的指导文件MEDDEV 2.7-1 rev 4,提出了等同的要求……

阅读更多 -
2021.03.01
有源医疗器械使用期限验证
任何类型的加速试验都是基于加速损伤理论。产品在生命周期内所承载的各种应力,会对产品造成渐进式的损伤累积,当损伤累积到一定量值,就会导致产品失效……

阅读更多 -
2021.02.23
生物医用高分子材料表征方法简介
生物医用高分子材料在医疗领域的应用越来越广泛,如常见的骨科植入材料、人工晶体、填充假体、人工血管、医用缝合线等等。生物医用材料,尤其是植入类材料,需要与人体长时间接触并在体内承担起修复和支撑功能……
阅读更多 -
2021.02.22
【独家】遵循ISO 14971:2019(医疗器械-风险管理对医疗器械的应用)
FMEA(潜在失效模式和后果分析)用于识别在产品设计或产品制造中潜在的失效模式。但是,医疗器械的相关风险并不仅仅是由失效造成的。一个产品可能永远不会故障,但仍有许多其他潜在风险。

阅读更多 -
2021.02.08
无菌医疗器械的生物、理化试验项目及要求
为确保无菌医疗器械的质量以及临床医疗使用的安全、有效,必须对其生产过程中的原料选择、配方、工艺流程、最终成品等进行一些检测,用于生产工艺过程的监控以及最终产品的放行……
阅读更多 -
2021.02.05
医用针式注射系统标准解读
药监局在2019年3月15日年印发2019年医疗器械行业标准制修订项目计划的通知(药监综械注〔2019〕23号)。通知中计划2019年修订93项医疗器械行业标准。此次由全国医用注射器(针)标准化技术委员会(SAC/TC 95)负责制定《医用针式注射系统要求和试验方法第1部分……
阅读更多












