谁说微针只能用一次?“凹”个造型试一试,医疗器械博览会速递这一技术
2023-06-29
微针(Microneedles,MN)是一种新型的物理促透技术,由多个微米级的细小针尖以阵列的方式连接在基座上组成,针体一般高10-2000微米、宽10-50微米。微针的长度、大小和形状可根据治疗的需求进行个体化设计。微针能定向穿过角质层,产生微米尺寸的机械通道,将药物直接置于表皮或上部真皮层,不用通过角质层即可参与微循环,发挥药理反应。
微针(MN)技术已成为替代基于血液的测试的替代方法,以获得更具成本效益、个性化、易于使用和快速报告的透皮传感设备,适用于实时生物标志物检测。MN的显着优势是它们可以轻松绕过皮肤的最外层并直接进入皮肤微循环或间质液(ISF),而不会刺破血管、损伤真皮神经。因此,基于MN或MN阵列技术的透皮电化学传感器正在成为健康监测和诊断中个性化可穿戴设备的前沿技术。
然而,透皮传感器的性能主要会受到位于MN表面的传感层的损坏或变形的影响,这通常是由于MN表面和皮肤组织之间产生的摩擦而发生的。为此,来自澳大利亚的蒙纳士大学的Nicolas H. Voelcker团队开发了一种4×4聚合物MN阵列(PMNA),其单个MN高度为~720 μm,并在MNs表面集成导电凹陷微腔(MC),以在插入和移除过程中保护传感层皮。作者利用猪皮进行了相关表征和概念验证,表明MNA的三维纳米结构为插入皮肤后保持性能的关键问题提供了替代解决方案。
相关研究成果以“Microneedles with Recessed Microcavities for Electrochemical Sensing in Dermal Interstitial Fluid”为题于近期发表在《ACS Materials Letters》上。
包括微针在内的更多注射器相关产品,尽在医疗器械博览会。曾在医疗器械博览会中亮相的过滤器和静脉注射产品供应商,包括颇尔药液/疏水呼吸通路过滤器、疏水性混合纤维素膜、自排气精密过滤器、4TipTM 系列吸头滤芯、血液透析器封装系统、鲁尔接头、微流量调节器等。
PMNA的设计如图1所示,这些MC是位于金字塔形MN尖端的导电微型袋,它可以(i)容纳传感层或生物识别元件并允许进行电化学分析技术,(ii)保护传感层在插入或移除,以及(iii)将传感层放置在皮肤(真皮)的适当深层以进行ISF访问。为了演示该方法,作者准备了一个生物传感器,该传感器由一个电极组成,该电极具有一个4×4 MN阵列,其中包含用葡萄糖氧化酶(GOx)修饰的MC。电极由涂有一层薄薄的Au(Au-PMNA)的生物相容性OrmoComp光刻胶制成(图1a),MC凹陷在MNs表面(Au-PMNA/MC)(图1b)。
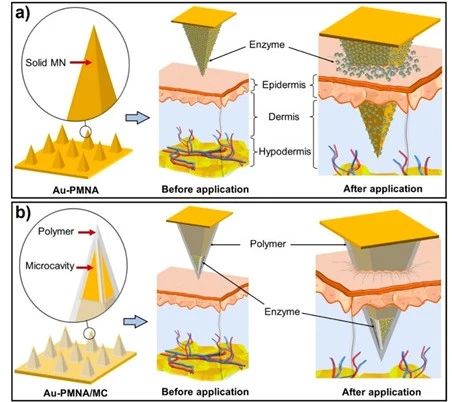
图1 PMNA的设计示意图
首先,通过SEM对掺入MC之前和之后的MN进行形态学表征。顶部(图2a)和倾斜(图2b)视图的SEM显微照片显示4×4的金字塔形MN阵列,间距约800 μm。Au-PMNA的侧视图显示MN高度为~680 μm,底部为~400 μm,MN尖端的锐度为~2.5 μm。图2c和d中的SEM显示成功制造的MC位于阵列中所有MN的尖端。MC位于金字塔形MN的每一侧(因此每个MN有4个MC),每个MC的底部约为100 μm,两侧约为200 μm,并且从OrmoComp 层的顶部凹进约20 μm 。在AuPMNA 表面上沉积薄的OrmoComp层导致尺寸发生变化,其中Au-PMNA/MC中的 MNs 具有~ 330 μm的底部和~ 720 μm的高度,而MN尖端的锐度大致保持不变(图2c、d)。

图2 微针的表面形貌
除了形态表征外,还使用电化学技术对电极制造和表面改性过程进行了表征。为了测试 Au-PMNA/MC 电极保护传感层的能力,实验使用猪皮进行研究,以观察 MNA 表面缺少 (Au-PMNA) 和存在 MC 对传感器响应的影响。用 GOx 酶修饰的 Au-PMNA(图1a)和Au-PMNA/MC(图1b)电极应用于猪皮肤,在此期间MNs受到摩擦,随后使用 CV、DPV 和 EIS 技术进行测试(图 3)。通过记录两个电极的信号进行电化学测量,Au-PMNA(图3a)和Au-PMNA/MC(图3b)的CV图表明,在固定GOx后,氧化还原峰的电流强度降低。这是由于酶层的表面阻挡作用,它降低了氧化还原探针到 Au 层的扩散动力学。
使用DPV技术观察到类似的行为,其中大部分记录低电容电流,提供高灵敏度。Au-PMNA(图3c)电极的DPV图清楚地显示峰值电流强度在在猪皮肤中插入MN后约为0.2 V,而对具有MC的MN没有观察到显着影响(图3d)。CV和DPV结果与EIS分析观察到的结果一致。根据EIS结果,固定GOx后Au-PMNA的Rct值从 70 ± 5增加到 275 ± 12 Ω,而在将MNs插入猪皮肤后这些值开始下降,表明酶从MN表面分层(图3e)。相反,Au-PMNA/MC 电极插入猪皮肤后的 Rct 值没有变化(图3f)。
总的来看,CV、DPV和EIS结果清楚地表明,凹陷MC的引入在刺穿皮肤以及从皮肤上去除MN期间保护传感层。
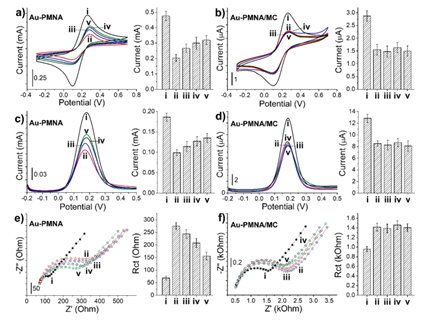
图3 电化学表征:CV、DPV和EIS
接着,AuPMNA和Au-PMNA/MC修饰的氧化石墨烯电极的拉曼光谱如图所示(图4a-b)。拉曼活性带的强度随着 Au-PMNA 电极的每次应用而降低,表明氧化石墨烯从MN表面损失。相反,Au-PMNA/MC 电极没有观察到统计学上的显着变化(图4b)。使用 GOx 修饰电极观察到类似的拉曼结果,其中 GOx 酶被氧化石墨烯非共价标记。此外,为了检测猪尸体皮肤表面的分层氧化石墨烯(图 4c),在 MN 应用前后对皮肤表面进行了分析。图 4d 显示了应用 AuPMNA/MC (ii) 和 Au-PMNA (iii) 电极之前 (i) 和之后猪皮肤的拉曼光谱,以及皮肤应用 (iv) 之前 Au-PMNA 表面上氧化石墨烯的参考光谱。参考样品 (iv) 中存在的氧化石墨烯拉曼活性带在 (i) 之前和应用具有凹陷 MC (ii) 的 MN 之后的猪皮肤样品上未观察到。但应用Au-PMNA电极 (iii)后的皮肤表面显示出明显的氧化石墨烯拉曼活性带,表明皮肤表面存在分层氧化石墨烯。图4中显示的结果与图3中显示的电化学测量结果一致,证实了凹陷MC的引入在皮肤穿刺和从皮肤上去除MN期间保护传感层的发现。
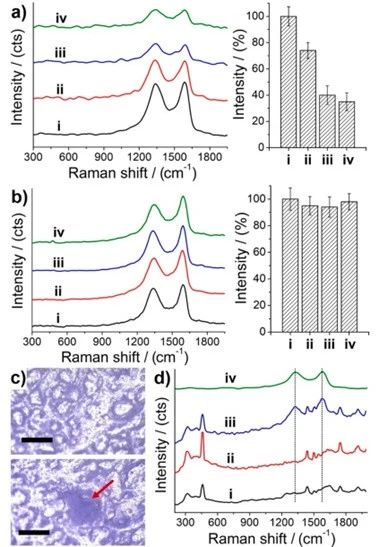
图4 (a) Au-PMNA 和 (b) Au-PMNA/MC电极的拉曼光谱
最后,作者通过记录 Au-PMNA-GOx的安培响应和Au-PMNA/MC-GOx电极在(i)之前和重复(ii, iii, (iv))应用于猪皮肤之前不同的葡萄糖浓度(图5)。Au-PMNA和Au-PMNA/MC 电极对在 10 mM PBS (pH 7.4)中以0.7 V记录的连续添加2 mM葡萄糖的安培响应如图5a和b所示。在第一次将 Au-PMNA 电极(图5a)应用于猪皮肤后,与(i)皮肤应用之前的传感器响应相比,电流响应急剧下降。随着第二次(iii)和第三次(iv) 皮肤插入,安培计反应继续下降,表明固定化GOx酶的损失或降解。然而,AuPMNA/MC-GOx电极(图5b)在第一次(i)或第一次(ii)、第二次(iii)或第三次(iv)皮肤应用之前没有显示安培响应的显着变化。从安培响应得出的校准曲线(图5c-d)可以看出 MC 的明显优势。
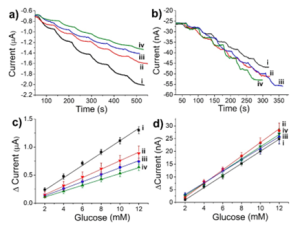
图5 (a)Au-PMNA-GOx 和(b) Au-PMNA/MC-GOx电极在猪皮上的安培测量
综上,本文报告了一种MNA的开发设计,重点是解决防止由MN表面和皮肤组织之间的摩擦引起的传感层损坏或变形的关键挑战。该MN表面具有集成和凹陷的MC,导电Au层位于MC内部,这使得适用于电化学测量的导电表面的功能化和生物识别元件在该表面上的固定化成为可能。最重要的是,与没有MC的MN不同,MC可以防止在皮肤插入和从皮肤移除过程中酶层的分层和变性,即使在多次皮肤应用后也是如此。Au-PMNA/MC传感平台的保留功能已通过猪皮测试和电化学测量成功证明。
医疗器械博览会了解到,除了为上述挑战提供解决方案外,这项工作还旨在为新型MNA奠定基础,其中涉及对MN表面进行工程设计以开发适合平移的透皮传感设备。这将通过克服挑战、降低可穿戴传感器制造过程的成本和时间以及提高基于MN的诊断和健康监测的可靠性来帮助推进透皮传感技术。
文章来源:https://doi.org/10.1021/acsmaterialslett.3c00441












