2022年苏州医疗器械展会骨科植入物材料研究报告 | 聚醚酮酮及其复合材料
2022-09-16
骨植入物指的是将骨头从骨骼的一块区域植入到另一块区域,以帮助治愈、加强和改善人体功能。骨头或类似骨头的材料用于骨植入物,可能取自患者自身供骨区或人造材料。在多数情况下,骨植入物用于填补因疾病、损伤、畸形或脊柱手术如融合术造成的椎骨之间的空隙。为了满足该领域的采购需求,2022年苏州医疗器械展会Medtec China 2022 16大特色展区,包括医用3D打印,骨科加工专区,及超精密激光加工、金属材料,部件和加工设备等研发设计领域,许多展商也将来到展会现场展示企业最新的产品及设计。
聚醚酮酮(polyetherketoneketone,PEKK)是一种在主链结构中含有两个酮键和一个醚键的重复单元的半晶体线性热塑性聚合物,具有接近人体天然骨的弹性模量、生物相容性和良好的化学稳定性、射线可透性、与MRI兼容等优点,是制备骨科植入物的新型生物材料,但其表面疏水性及生物惰性限制了其应用。通过特定的材料制备工艺制造出既能保留甚至提升PEKK原有性能又能提高其骨生物活性的复合材料是当前骨科植入物的研究热点。PEKK复合生物陶瓷(如羟基磷灰石、氮化硅)以及生物相容较好的金属(如钽、铝和钛)制备的复合材料,不仅保持了与人体骨骼相似的弹性模量、提升了硬度,还改善了生物相容性、增加了抑菌性能及促进骨整合等能力,在骨科植入物领域非常有发展潜力。通过检索PubMed、Embase、ScienceDirect、中国知网及万方数据库中有关PEKK及其复合材料在生物医学领域中的应用研究,分析近年来PEKK及经过不同改性策略(如掺杂混合物改性、表面磺化改性、3D打印以及表面沉积技术处理等方法)的复合材料的特性、优势及不足,为制备满足临床需求的具有多种功能的骨科植入物提供参考。
随着人口老龄化加剧、交通伤以及运动损伤的增加,临床上骨科植入物的需求也在不断增长[1]。常用的骨科植入物材料包括陶瓷、金属、聚合物和复合材料。陶瓷材料主要有羟基磷灰石(hydroxyapatite,HA)、β-磷酸三钙以及氮化硅(Si3N4,SN)等,具有刚度高、脆性大、韧性差,不能在承重部位使用的特点,因此限制了其在骨科植入物中的应用[2,3,4]。常见的金属材料,如钛合金、钴铬钼合金和316L不锈钢,具有优异的机械强度和延展性,通常用于承重骨替换、脊柱融合及骨固定装置[5,6,7]。但这些金属植入物也存在一定的缺陷,如应力遮挡效应、腐蚀问题以及术后的植入物检测受限等。金属植入物的弹性模量显著高于人皮质骨,因此植入物周围骨组织所受的应力刺激明显低于骨组织维持自身更新所需的应力刺激,导致植入物周围部分骨组织吸收、强度降低、植入物松动,最终造成植入失败,即产生所谓的应力遮挡效应[8]。腐蚀是由于植入物与体液的相互作用,使金属离子释放,引起机体过敏、炎症和细胞毒性反应。另外,金属植入物与MRI、CT等影像技术不兼容,不利于对植入后骨生长及愈合进行监控[9]。聚合物和复合材料因易加工性、良好的化学稳定性以及较轻的重量而成为具有应用前景的骨科植入物材料。聚合物分为可生物降解聚合物(如聚乳酸、聚乙醇酸及其共聚物)和不可降解聚合物[如聚芳基醚酮(polyaryletherketone,PAEK)]。虽然可生物降解聚合物能应用于组织工程支架和合成骨移植替代品,但不适用于永久性植入物固定,因此不可降解聚合物在临床上仍然具有巨大的需求[10]。
不可降解聚合物中的代表PAEK是一种高温热塑性聚合物,具有良好的生物相容性、化学稳定性、高机械强度、射线可透性以及与MRI兼容等特点,目前已逐渐成为骨科领域常用的植入物材料。PAEK家族具有代表性的有聚醚醚酮(polyetheretherketone,PEEK)、聚醚酮酮(polyetherketoneketone,PEKK),其中碳纤维增强聚醚醚酮(CFR-PEEK)与人体骨骼具有相近的模量,良好的生物相容性,和较低的密度,是近年有望替代刚性金属植入物的新兴高分子骨植入材料。植入物的实时应变评估对于骨折伤患处愈合和植入物服役状态的术后监测起到至关重要的作用,然而如何将高精度和服役稳定的传感器集成在骨科植入物上仍然是较大挑战。
PEKK是一种半晶体线性热塑性聚合物,含有由芳香环桥接的碳基和醚基团,由Bonner于1962年首次合成。与PEEK相比,PEKK除具有更高的热稳定性和机械性能外,还同时具有更多的酮基,允许更多的表面化学改性选择[12,13]。例如,PEKK可作为脊柱植入物,如笼、棒和螺钉,维持脊柱的刚性稳定,使脊柱骨骼融合。与传统的金属植入物相比,PEKK植入物在脊柱融合中可以避免应力遮挡和假体下沉等严重问题的发生[14]。另外,PEKK还可通过3D打印技术制备出适配的植入物用于人工关节置换和骨缺损的治疗。随着生物工程学、材料学、机械制造技术等相关学科的飞速发展,PEKK及其复合材料的生物活性和力学性能也在不断改进,并有望应用于创伤和组织工程支架等领域。
骨科植入物植入人体后,骨-植入物界面的骨整合不良对植入物与宿主周围组织的整体性有重要影响。因此,增强骨科植入物的骨整合和骨诱导能力是外科医生、化学家和材料学家的研究热点。如PEKK植入物光滑且疏水的表面使其具有生物惰性,导致与周围骨组织结合的能力差,从而限制了其在骨科植入物中的应用。本文综述近年来PEKK及经过不同改性策略的复合材料的优势及不足,同时也分享了一种新型的碳纤维增强聚醚醚酮(CFR-PEEK)材料,为制备满足各种需求的具有多种功能的骨科植入物提供参考。
骨科替代植入物:
骨植入替代物包括:
脱钙骨基质(DBM)– 是一种加工过的同种异体骨植入物。DBM包含从同种异体骨植入物提取的胶原蛋白、蛋白质和生长因子。脱钙骨基质的形态主要为粉末、颗粒、小块,可以通过注射器注射。DBM已经被广泛加工,基本没有疾病传染的风险。但是其存在形式不能为手术部位提供支持。
陶瓷– 陶瓷也用于骨植入物的替代物。陶瓷不存有任何疾病传染的可能性,但是可能导致一些患者术后发生炎症。陶瓷替代物有多种形式,如多孔和网眼状。尽管陶瓷可能会为骨生长提供框架,它们不含任何影响骨生长的天然蛋白质。
珊瑚– 珊瑚制成的骨植入物已经证实对治疗因创伤、肿瘤和囊肿引起的骨缺损有效。它还作为植入扩充物用于脊柱手术,或者作为植入物,为骨生长提供框架。使用这些替代物在某些特定条件下具有良好结果。
植入物复合材料–这是骨植入替代物的较新领域,植入物复合材料使用其他骨植入材料和/ 或骨生长因子的复合物 ,从而汲取各种物质的优点。在各种使用的复合物中,胶原蛋白/陶瓷复合材料可以生产天然骨成分;DBM及骨髓细胞有助于新骨的生长;以及胶原蛋白/陶瓷/自体植入复合物。
骨形态发生蛋白(BMP)– 骨形态发生蛋白由人体产生,并且可以控制骨形成和治愈。 科学家发现,这些蛋白能够加速治愈并且限制一些患者的同种异体骨植入和非骨植入物的不良反应。科学家还发现,从人体和牛的骨头上提取这些替代物,甚至可以在实验室制作骨形态发生蛋白。目前,美国食品与药物管理局还没有批准这些治疗方法;但是,人们正在对人类和动物开展广泛研究,确定其安全性和有效性。
PEKK及其复合材料的改性策略
为满足PEKK及其复合材料作为骨科植入物材料的需求,大量文献介绍了PEKK的改性策略,如掺杂生物活性物质、3D打印技术、冷喷涂、飞秒激光(femtosecond laser,FSL)技术以及化学反应处理(如磺化作用),用以提高PEKK及其复合材料的机械性能、生物相容性及骨整合能力。
(一)PEKK混合物的掺杂改性
PEKK表面具有疏水性和生物惰性,使PEKK能够在保持原有优势的情况下通过混合掺杂改性的方法改善其复合物的性能,从而具有优异的生物相容性、抗菌活性及骨整合能力。常见的PEKK填充颗粒包括HA、SN、钽(Ta)等。
人骨组织是一种生物复合材料,由纳米羟基磷灰石(Nano hydroxyapatite,NHA)、胶原纤维及骨细胞组成。而HA与人类骨骼和牙齿的矿物成分接近,掺杂HA可提高PEKK的机械强度、刚度及生物相容性。PEKK与生物活性物质最常用的掺杂方法为共混,但通过共混制备的复合材料存在生物活性物质团聚以及含量难以提高的问题。因此,这种制备方法还需要改进,以保证复合材料中的生物活性成分分散均匀,并提高其含量。杨雪勤等[15]在常温、常压下通过傅克反应合成PEKK,即在合成PEKK的过程中加入了HA,让部分PEKK在HA表面生成,使其能够均匀包裹在HA表面,从而合成了与人体骨骼相近的HA质量分数高达50%的PEKK/HA复合材料;将复合材料的载荷、模量和硬度与人体骨骼进行对比,发现复合材料的性能与人体骨骼几乎相同,说明其与人体骨骼有较好的力学匹配性;细胞毒性试验证实该复合材料无细胞毒性,并对细胞增殖有一定的促进作用,具备优异的生物相容性。因此,通过傅克反应生成的PEKK/HA复合材料,不仅可保证复合材料中生物活性成分均匀分散,还能提高其含量,使其拥有优异的力学匹配性和生物相容性,具有制备骨科植入物的潜力。SN作为一种生物医学陶瓷,自1989年开始被广泛研究。SN的特点是机械强度大、耐腐蚀性强,并具有良好的生物相容性、抗菌活性和骨整合能力,从而成为骨科植入物的候选材料[16]。细菌感染是造成植入物失败的一个主要原因。为了通过增强PEKK的抗菌活性和骨整合能力来提高植入物的成功率,Wu等[17]在PEKK表面合成了PEKK/SN复合材料的微孔涂层,并将制成的复合材料植入兔股骨缺损模型。研究结果表明,微孔镀液中SN的含量随浓硫酸悬浮液中SN的含量增加而增加(浓硫酸中没有SN的为PKS,PKSC5和PKSC10中SN的含量分别为5%和10%),并且随SN含量增加PEKK上微孔涂层的表面粗糙度和亲水性显著提高。表面亲水性提高不仅适合细胞黏附及增殖,而且还有利于植入体内新骨组织的生长。此外,由于氨基(-NH2)和磺酸(-SO3H)的协同作用,PKSC10的微孔涂层表现出良好的抗菌活性及蛋白质吸附改善。其中蛋白质在生物材料表面的吸附有利于细胞黏附,可促进细胞膜与生物材料的接触和伪足的延伸;蛋白质在生物材料表面吸附的增加可减少细菌黏附、抑制细菌生物膜的形成,从而表现出优异的抗菌活性。因此,高SN含量的PKSC10微孔涂层具有良好的生物相容性、抗菌活性以及骨整合能力。
若想了解更多有关人工关节等骨科相关的热点话题,加入2022年苏州医疗器械展会Medtec China 2022 16大特色展区“第八届植入介入医疗器械中国峰会”,来自北京大学等高校的嘉宾将讲解金属植介入器械产品中的医工结合。议题覆盖金属骨科植入物的材料选择、产品设计与生物学评价、金属心血管介入器械的材料选择、产品设计与生物学评价等。点击快速预登记。
近几十年来的研究证实,与不锈钢和钛(Ti)相比,Ta具有优异的生物相容性、耐腐蚀性和低细菌黏附性,同时其纳米结构薄膜不仅可促进细胞黏附,而且还具有出色的抗菌活性[18],因此作为可植入材料在骨科植入物领域越来越受到关注。Hu等[19]结合PEKK和Ta的优点,将PEKK与体积分数20%(PT20)和40%(PT40)的Ta微粒混合制造PEKK/Ta可植入复合材料;研究发现,与PT20和纯PEKK相比,PT40由于Ta含量较高而使表面亲水性、粗糙度、蛋白质吸附能力以及机械性能显著提高;PT40还表现出略优于人类皮质骨的机械性能(如压缩强度和弹性模量更高),显著改善了体内的骨形成和骨整合。因此,将Ta微粒掺入PEKK制备出具有改进表面性能的可植入复合材料,在刺激细胞反应、改善骨形成以及骨整合方面可发挥积极作用。
相比于普通的二元掺杂混合改性方法,多元掺杂混合改性可以更好地提高PEKK性能。为了使PEKK满足新型生物活性植入物的需求,拥有优异的机械性能、抗菌活性及骨整合能力,Hu等[20]将PEKK浸入含有SN和Ta微粒的浓硫酸悬浮液中,制备出表面微孔中含有SN和Ta微粒的复合物STP。研究结果证实,与不含微粒的磺化PEKK相比,其粗糙度、亲水性和蛋白质吸附大幅增加,可以显著诱导大鼠骨髓间质干细胞的增殖和分化,促进新骨再生和骨整合;在体外诱导细胞反应和体内骨整合改善方面,含Ta的微孔表面优于含SN的微孔表面;另外,由于SN微粒的存在,STP还表现出优异的抗菌活性,在体外可抑制细菌生长、在体内可防止细菌感染。总之,通过多元掺杂混合改性的STP具有良好的成骨和抗菌双重生物功能,在骨科植入物领域显示出巨大的潜力,这也为研究通过多元掺杂混合改性提高PEKK的性能提供了新的思路。
(二)表面磺化改性
骨科植入物感染是常见并发症,造成植入物失败主要由其周围炎症导致,与其表面形成的细菌生物膜降低植入物表面的生物相容性引发的骨吸收密切相关。研究人员认为通过磺化可以将磺基团引入PAEK材料的表面,不但增强了复合材料的抗菌活性,还能提高其表面的亲水性和孔隙率。亲水表面和孔隙率的增加有利于细胞增殖和黏附,从而加速骨形成和植入物的早期骨整合[21]。许多研究表明,可以通过各种技术增加复合物支架高水平的互联孔隙度、减轻机械错配、促进骨整合和射线可透性来改善永久性植入物的固定[22]。Yuan等[23]采用HA微球成孔剂浸出法制备出多孔PEKK支架——PEKK-P,再对其表面进行磺化处理制备出复合物PEKK-SP,使其同时具有相互连接和开放的大孔(200~600 μm)及微孔(< 10 μm)。其中大孔由HA微粒产生,而微孔经磺化后形成;最后经模拟体液(simulated body fluid,SBF)浸泡5 d,制备出内部和表面都形成致密的骨样磷灰石层的复合物PEKK-BSP。通过体外细胞实验及体内大鼠股骨缺损模型研究发现,PEKK-BSP的力学稳定性和生物相容性显著优于PEKK-P及PEKK-SP。因此,经特殊物理和化学处理表面改性的多孔PEKK作为骨科植入物在骨缺损应用中具有巨大的潜力。为了比较PAEK家族中PEEK与PEKK的差异,随后Yuan等[13]又用此联合方法制备了PEEK的复合物PEEK-BSP。结果证实PEKK-BSP和PEEK-BSP具有相似的宏观结构,但由于PEKK上的酮基团多于PEEK,因此经过磺化处理后PEKK-SP不仅有较高浓度的-SO3H基团,而且其表面的微孔也明显较PEEK-SP多而在SBF浸泡过程中磷灰石沉积的速度较PEEK-SP更快、骨整合能力更强。因此他们认为,与PEEK相比,PEKK的化学结构允许更多的表面修饰,可增强其抗菌活性以及增加细胞与蛋白质的黏附,因此更适合作为骨科植入物。Xiao等[24]对3D打印的PEKK支架进行了磺化处理,并在支架上制备了钛生物活性涂层,以提高其生物活性。即首先通过磺化处理将-SO3H基团带到PEKK表面,为钛涂层的锚定提供了更多的成核点;随后采用水热法沉积二氧化钛纳米结构,提高PEKK的生物活性;在前体溶液中处理,一方面弱负电荷的样品表面在SBF中表现出优异的磷灰石形成能力,另一方面留在磺化处理后的PEKK表面的磺酸产物被隐藏起来使表面亲水性大幅提高,从而促进细胞的黏附和增殖。因此,表面磺化改性可以作为提高3D打印定制PEKK复合材料生物活性的新方法。 (三)3D打印PEKK支架材料 随着增材制造技术的进步,在骨缺损修复、脊柱融合、人工关节置换方面,3D打印技术可在CT成像的基础上为患者定制解剖结构假体,更好地恢复功能和提高生活质量。PEKK是一种可打印的,具有生物相容性、化学稳定性及与人体骨骼相似的力学性能的特殊材料。此外,它还具有射线可透性,可监测植入物位置,对其进行预后评估。通过选择性激光烧结(selective laser sintering,SLS)打印的PEKK已被美国食品和药物管理局批准用于骨科领域。SLS打印PEKK具有许多优点,如可以简易、快速以及高精度地制作植入物,方便供体细胞植入等。PEKK的局限性在于低骨诱导性,这一点可以通过加入生物活性因子来改善。Roskies等[25]在3D打印的多孔PEKK支架中添加脂肪干细胞(adipose stem cells,ADSCs),通过动物实验、组织学观察证实了PEKK/ADSCs复合材料在兔下颌骨缺陷中的整合能力。由于Landy等[26]发现孔隙率为50%、平均孔径为100 μm的PEEK支架可促进成骨细胞分化,而且有研究表明孔径>100 μm的支架可诱导间质干细胞分化[27],因此有研究者制造了孔隙率为50%、平均孔径为730 μm的PEKK支架,并通过体外碱性磷酸酶实验证实ADSCs在多孔PEKK支架中培养具有优越的分化能力。这一结果归因于3D打印支架的多孔结构促进了营养物质流动和细胞迁移,并通过旁分泌信号刺激进一步改善了骨分化[25]。在骨科临床中,通过3D打印技术可以精确制备出与人体高度匹配且性能优异的假体,提高手术成功率及术后疗效。3D打印技术应用于肋骨假体、全膝关节假体及椎间融合器,可以对PEKK进行表面改性,如改变材料表面微纳米结构、提高材料表面的亲水性、制备生物相容性较好的表面涂层等;为了改善PEKK支架材料的机械性能,还可以通过复合其他材料,如HA、碳纤维,以及将生物活性因子(如ADSCs、人滑囊液间质干细胞)植入3D打印PEKK支架,增强植入物的生物相容性及骨再生能力。未来随着3D打印技术的发展以及对PEKK研究的深入,将研制出各种满足于骨科临床应用的植入物。
2022年苏州医疗器械展会Medtec China技术论坛A:医疗器械诞生的助推器——创新医用材料/配件及精加工(一)议题覆盖医用塑料在医疗器械生产过程中的应用、汉高医疗行业创新解决方案、埃万特医疗级聚合物解决方案如何为您的体外诊断(IVD)应用增加价值、蔻兰多彩高性能材料解决方案在医疗行业的应用等。
(四)表面沉积技术处理
对复合材料表面可以进行金属化处理,常见的方法有物理气相沉积(physical vapor deposition,PVD)、化学气相沉积(chemical vapor deposition,CVD)、化学镀、热喷涂技术、高速氧燃料和等离子喷涂技术。虽然热喷涂技术、PVD、CVD和电镀工艺沉积率更高,但原料粉末在沉积过程中发生熔化可产生两种不利的影响:首先沉积物产生热诱导的残余应力同时伴随着氧化反应,其次熔化的液滴会损坏复合材料基板。因此,热喷涂并不适用于聚合物和复合基材。随着制造技术的不断突破、创新,另一种粉末沉积工艺——冷喷涂可能更适用于将金属沉积在热敏基板上。冷喷涂是一种固态粉末沉积过程,金属粉末通过超声波气体流加速沉积到基体上;发生撞击后粉末会经历严重的塑性变形,并有效地熔断(冷焊),以产生完全稠密的沉积物。一些研究表明,在冷喷涂层制备过程中温度较低,可避免金属氧化以及对基体不良的热作用,因此对热塑性材料进行表面沉积处理具有较大优势[28,29]。Feng等[30]采用高压冷喷涂将铝沉积在PEKK-30%短碳纤维基体上,实现了冷喷涂技术对PEKK表面进行金属化处理。冷喷涂还可在较低的温度下在PEKK基体表面制备出厚度均匀且与基体有较强结合力的涂层,喷涂过程迅速、无污染,不仅增加了基体材料的机械性能和生物相容性,还增强了PEKK与涂层的黏合强度。因此,冷喷涂作为一种骨科植入物涂层制备新技术,具有巨大的应用潜力。
FSL技术是一种应用前景广阔的微纳米结构制造技术,具有加工简易、精度高、扫描速率快、加工过程中材料表面氧化程度小等优点,能在多种材料表面(包括金属、陶瓷、玻璃和高分子材料)高效构建可控的微纳米结构来调控细胞行为(如黏附、增殖和分化等)[31]。Wu等[32]在PEKK/SN生物活性复合材料上进行FSL处理,在植入物表面创建微纳米结构,显著提高了复合材料的粗糙度、亲水性、表面化学基团(如-NH2)含量以及蛋白质吸附能力;并在兔股骨空洞缺损模型中表现出更强的生物相容性、抗菌活性、成骨活性和骨整合能力。因此,经FSL打造出具有微纳米结构的PEKK,可以提高骨科植入物的抗菌活性及骨整合能力。
三、不同改性策略的优势与不足
为了满足PEKK及其复合材料作为植入物材料在骨科领域中的应用,催生了大量的方法用以提高PEKK的机械性能、生物相容性及骨整合能力。通过掺杂生物活性物质,如生物陶瓷中的HA、SN和金属中的Ta、铝及钛有助于改善PEKK的机械性能、生物相容性及骨整合能力,增强其抗菌活性及蛋白质吸附能力,还可以通过多元掺杂改性的方法来实现不同功能;3D打印技术可以通过对PEKK基体结构进行改性,并根据患者需求精确打造理想的植入物假体,在增加合适孔隙率的同时还可以对其进行生物活性因子功能化处理,如ADSCs和人滑囊液间质干细胞,促进新骨向植入物内生长,增强植入物在体内固定的稳定性;冷喷涂更适用于热塑性材料,将金属粉末通过超声波气体流加速沉积到基体,在其表面形成致密的涂层,提高金属涂层与基体表面的黏合强度;FSL技术能在植入物表面简易高效地构建可控的微纳米结构来调控细胞行为,如细胞黏附、增殖和分化等,增加基体材料的抗菌性及骨整合能力;化学反应处理如磺化作用,可在植入物表面形成微孔,增加植入物表面的粗糙度和孔隙率,促进细胞黏附、增殖和分化,并将磺基团引入基体表面提高植入物的亲水性、抗菌活性及骨整合能力。
在复合植入物的制备过程中常常会遇到一些问题,如在混合物掺杂过程中PEKK与生物活性物质分散不均匀以及含量难以提高;生物活性涂层(如HA涂层)与植入物基体表面的黏合强度较弱,导致其从PEKK表面脱落而引发炎症;复合材料改性过程中添加材料与基体之间的相容性差,引起复合植入物整体机械性能降低;移植特定的官能团对植入物进行功能化处理可以改善PEKK的生物特性,但其性质通常不稳定;喷砂处理虽然可以提高植入物表面的粗糙度,有利于细胞反应,但PEKK生物惰性的本质并未得到解决;尽管有些基于PEKK的植入物已显示出短期稳定性和良好的临床结果,但长期性能和稳定性仍然有待观察。
四.基于激光直写的CFR-PEEK智能骨科植入物
近期,清华大学机械工程系臧浠凝助理教授(特别研究员)团队通过激光直写的方法,无需粘合剂或固定装置,直接在CFR-PEEK表面上原位制备出了应变传感器(图1)。该工作首先从激光与CFR-PEEK和PEEK相互作用的研究入手,通过改变激光的能量密度,实现了表面碳化物的形貌(图2a-b)、成分(图2c)和面电阻的可控加工(图2d)。通过激光参数的调控,可使最小面电阻小于1.7 Ω sq-1。
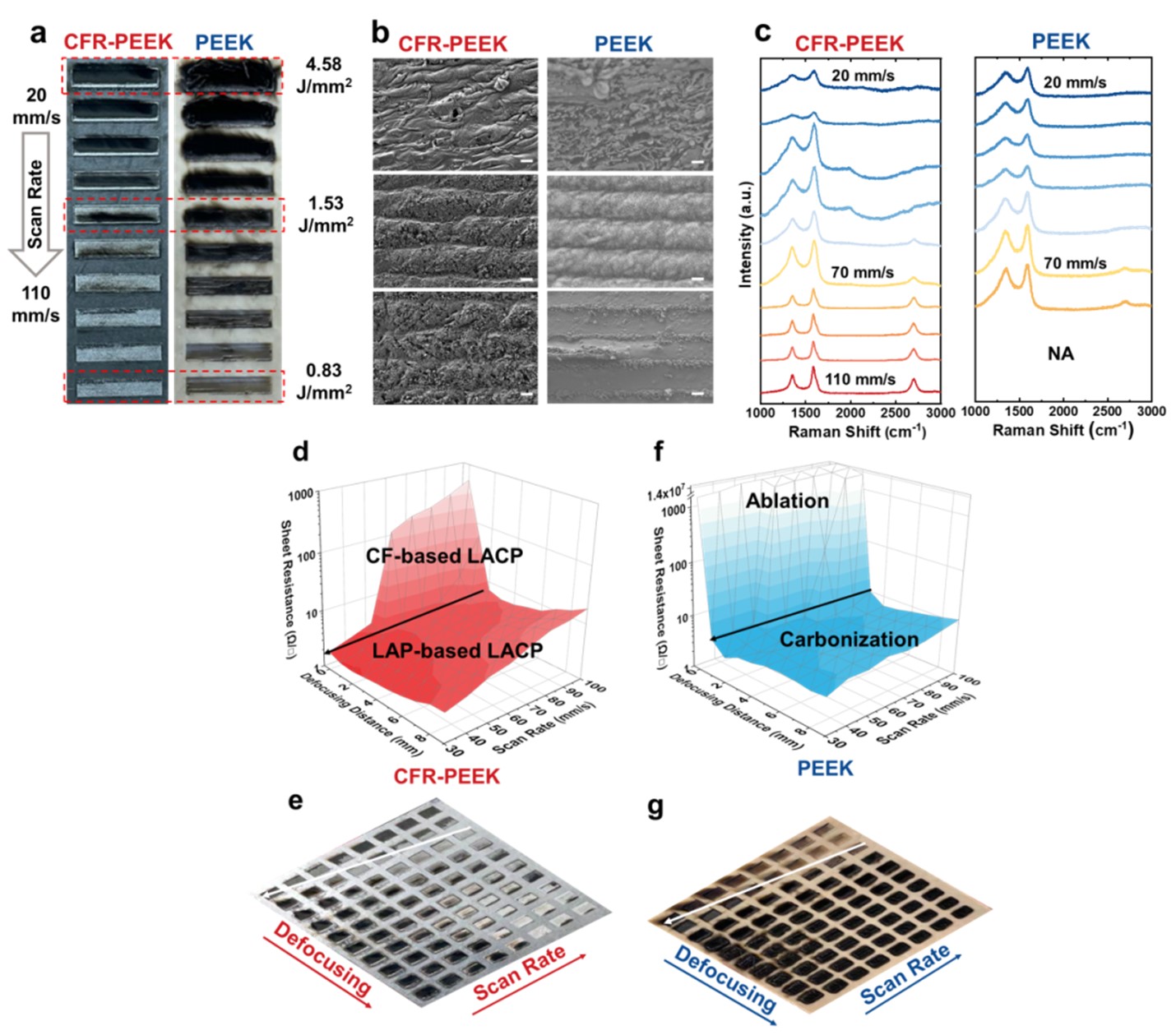
图2. 激光与CFR-PEEK和PEEK相互作用的研究:a-b)激光能量密度对表面碳化物形貌的影响,c)激光能量密度对碳化物成分的影响,d)激光参数对碳化物面电阻的影响。
在相互作用研究和可控加工的基础上,团队成员制备出了CFR-PEEK基应变传感器。实验发现,传感器在CFE-PEEK植入物的全服役范围内(约0-2.5%)均能保持较好的线性度(R2 = 0.997)(图3a);通过低周应变循环下传感器表面形貌变化的研究,团队成员揭示了传感器的工作机理(图3b)。通过将传感器与蓝牙模块相连,该传感器可以实现无线信号传输,进而在移动设备终端进行显示(图3c-d),未来有望实现骨折病人术后便捷随访以及康复信息的云共享。

图3. CFR-PEEK基骨植入物应变传感器:a)灵敏度和线性度测试,b)低周应变循环下电阻和表面形貌的变化,c-d)传感器连接蓝牙装置与移动设备无线通讯。
该项工作利用六轴商用机械臂级联激光头,实现了在CFR-PEEK基骨植入物任意曲面上的传感器的加工(图4a)。所制备的传感器在一定应变范围内依然具备较好的线性度(图4b)和稳定性(图4c),未来通过机械臂和激光头的参数协同优化,使3D曲面传感器性能有望达到平面加工效果。

图4 a)机械臂加工系统,b)机械臂加工传感器灵敏度测试,c)传感器稳定性测试。
五、总结与展望
PEKK虽然已经成为具有广泛应用前景的骨科植入物材料,但其本质上具有生物惰性,同时植入物周围纤维组织包裹的形成和弱骨整合能力等缺点是制约其进一步发展和应用的瓶颈。因此,为了满足作为植入物材料在骨科领域中应用的需求,我们通过分析改变PEKK结构和使PEKK表面功能化的策略及其优势与不足发现,集成多种改性方法似乎是解决这一问题的可行方式。根据既往研究结果,我们认为首先可以通过傅克反应合成HA质量分数高达50%的PEKK/HA复合材料,解决复合材料与生物活性物质分散不均匀和含量难以提高的问题;再对其进行磺化处理,从本质上增加复合材料的孔隙率,提高植入物的亲水性、骨整合能力及抗菌活性;然后在其表面进行冷喷涂Ta涂层,增强生物活性涂层与植入物基体表面的黏合强度以及植入物的机械性能;最后对Ta涂层表面进行FSL处理,构建理想的微纳米结构以增加植入物的表面粗糙度,增强植入物的耐蚀性和抗磨损性能[15,23,30,32]。随着材料制备和表面改性技术的日趋进步,解决PEKK及其复合材料作为骨科植入物适用于临床实际应用的问题正逐渐变为现实。
来源:
中华骨科杂志
AdvancedScienceNews
中国医师协会骨科分会












