法规政策
-
2018.09.04
《医疗器械不良事件监测和再评价管理办法》发布
为加强医疗器械不良事件监测与再评价,及时有效控制医疗器械上市后风险,近日,国家市场监督管理总局和国家卫生健康委员会联合发布《医疗器械不良事件监测和再评价管理办法》(总局令第1号,以下简称《办法》)。《办法》2019年1月1日起施行。
阅读更多 -
2018.08.27
刚刚!国家市场总局一纸通知,医疗器械最严溯源监管时代来了!
一械一码,全国范围内建立起以唯一器械标识(UDI)为手段的统一追溯体系,就相当于任何一个医疗器械都有了唯一一张“身份证”! 医疗器械从生产、加工到流通、配送、使用全流程可溯源、全过程监管时代真的要来了!

阅读更多 -
2018.08.23
GB/T 19973.1-2015 标准解读
各个组织机构对警戒限和纠偏限的理解有所差异,该文对此进行分析比较,结合作者的理解给出了警戒限和纠偏限的定义;对合理确定警戒限和纠偏限的实施要点以及超出警戒限和纠偏限的调查进行总结概括;最后针对生物负载测定与医疗保健产品灭菌标准关系进行阐述。通过该文介绍,使读者更深刻理解GB/T19973.1-2015 的意义。
阅读更多 -
2018.08.20
医疗器械注册审评将有八大改革措施
公开审评要求 近几年,中心为指导申请人研发、规范内部审评尺度,不断加大指导原则的编制力度。组织完成十三五规划要求的200项医疗器械技术审查指导原则制修订编制工作,2017年
阅读更多 -
2018.08.15
医疗器械的数据完整性
数据完整性是当前医疗器械监管的重点,其本质就是从企业业务数据层面出发,通过观察业务数据本身的详尽程度、数据与数据之间的逻辑关系以及数据安全受控状态来判断其对应的业务执行的真实情况。文章从各国监管 机构对数据完整性的定义出发,分析其监管本质,企业实际现状以及其背后的原因,并最终找出企业因对方案。
阅读更多 -
医疗器械注册审评将有八大改革措施
近几年,中心为指导申请人研发、规范内部审评尺度,不断加大指导原则的编制力度。组织完成“十三五”规划要求的200项医疗器械技术审查指导原则制修订编制工作,2017年已完成52项,2018年计划完成61项。同时,中心将技术审查指导原则纳入审评质量管理体系管理,并以此为手段,统一全国各地各级审查标准和审评要求,推动全国技术审评的统一工作。
阅读更多 -
2018.08.08
新修订的《医疗器械分类目录》实施意义
8月1日,新修订的《医疗器械分类目录》正式施行。新规落地,对医疗器械监管提出新的要求。业内分析

阅读更多 -
2018.08.02
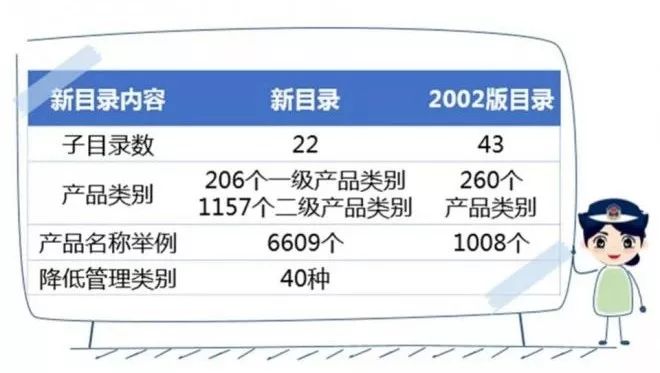
今日起执行!国家药监局新规落地,彻底影响医械企业!
万众期待的新版医疗器械分类目录今日起实施!新目录有哪些变化,对医疗器械生产经营企业又有哪些影响呢?
阅读更多 -
2018.07.30
医疗器械是否应该有失效期?
含有很精密电子设备的可植入医疗器械的使用时间比以前长,为了安全和责任,准入的门槛也在提高。

阅读更多 -
2018.07.27
关于设计历史文件vs. 510(k) vs. 技术文件:医疗器械开发人员需要了解哪些知识?
作为医疗器械领域的从业人员,你需要知晓许多的技术术语、文件和首字缩写词。有三种类型的文件容易让人产生混淆:设计历史文件、510(k)申报文件和技术文件。

阅读更多












