法规政策
-
2019.03.26
医疗器械相关的预期用途、适应范围、适应症的异同
“适用范围”“适应症”“预期用途”是医疗器械的注册审评审批中经常使用到的三个名词术语,并且在临床使用方面有着不同的意义。目前无论我国还是国外主要医疗器械监管机构对上述的概念缺少明确的辨析和区分,在上述名词的使用上存在一定程度的概念不清的问题。
阅读更多 -
2019.03.21
北京:创新医疗器械审批时间大幅缩短
记者日前从北京市药监局获悉,近年来北京不断优化营商环境,大幅压减创新医疗器械审评审批时间。 据悉,自《创新医疗器械特别审批程序(试行)》2014年发布以来,截至2018年底,
阅读更多 -
威高率先实施UDI管理——全面了解UDI及相关资料
近日,威高医用制品公司宣布,已经完成了威高医疗器械唯一标识(以下简称“UDI”)所有的技术论证工作,所有产品的UDI编码工作已结束,建立了威高的UDI数据库,数据库与ERP系统和MES系统关联,实现了数据的共享与交互。至此,UDI工作提前进入到了实施阶段,威高医用制品公司在国内同行业率先实施了UDI管理。
阅读更多 -
2019.03.14
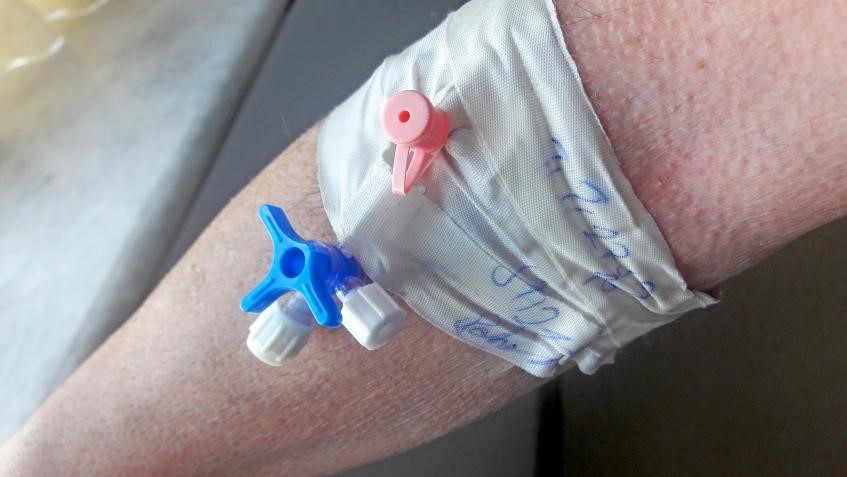
ISO 80369: 常见问题解答
以下是关于开发和测试小口径连接器的一些常见问题的解答。
阅读更多 -
2019.03.13
关于欧盟MDR你必须知道的8件事
在最近一项关于欧盟新法规的问卷调查中,调查参与者的回答让人不禁对推出该项法规的时机是否成熟表示担忧。你准备好了吗?

阅读更多 -
2019.03.07
2019“医疗器械注册人制度”大提速!这场“解绑”变革,距离真正颠覆还有多远?
近期,国务院一则批复——“开展医疗器械注册人制度试点,允许北京市医疗器械注册人委托京津冀地区医疗器械生产企业生产医疗器械”,引起了业内广泛关注。
阅读更多 -
2019.02.28
我国医疗器械上市许可持有人制度的构建与完善(上)
2017年10月8日,中共中央办公厅和国务院办公厅联合印发《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,提出要总结药品上市许可持有人制度试点经验,加强药品医疗器械
阅读更多 -
我国医疗器械上市许可持有人制度的构建与完善(下)
构建医疗器械上市许可持有人制度并非是一时的洞见和创意,而是有着长远的构建背景和设计过程。 2013年8月30日,第十二届全国人大常委会第四次会议通过了《全国人民代表大会常务
阅读更多 -
2019.02.25
国外医疗器械注册审评项目管理人制度研究及启示
span style=”font-weight:normal;”>2017年,中共中央办公厅和国务院办公厅印发《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,其中要求完善医疗器械注册审评项目管理人制度。笔者比较了美国、欧盟审评机构对项目管理的组织结构设计,验证了不同组织结构对我国审评机构的适用性,认为以专业为导向、兼顾效率的组织结构更加适用于我国。
阅读更多 -
更新生物相容性测试方法的另一个理由:欧盟新医疗器械法规
本文中化学和生物相容性领域的专家Matthew Jorgensen博士分享了在医疗器械生物相容性方面的最新见解和预测。

阅读更多












